托珠单抗治疗难治性全身型幼年特发性关节炎疗效及安全性
作者:文阅期刊网 来源:文阅编辑中心 日期:2021-11-17 08:27人气:
摘 要:目的:探讨托珠单抗治疗难治性全身型幼年特发性关节炎(SoJIA)的疗效及安全性。方法:选取2017年1月至2019年7月我院收治的41例难治性SoJIA患儿,均采用托珠单抗治疗,观察患儿治疗前后临床表现、实验室指标、关节功能变化情况,并对其疗效、安全性进行评价。结果:治疗后1个月、3个月、12个月患儿发热、皮疹、淋巴结肿大、关节炎比例均低于治疗前(P<0.05);治疗后1个月、3个月、12个月白细胞(WBC)、血小板(PLT)、红细胞沉降速率(ESR)、超敏C反应蛋白(hsCRP)水平均低于治疗前,血红蛋白(Hb)水平均高于治疗前,其中治疗后3个月、12个月的WBC、ESR水平均低于治疗后1个月,Hb水平均高于治疗后1个月;治疗后3个月、12个月美国风湿病学会(ACR)儿科(Ped)关节功能评价系统ACR Ped 30、50、70转化率均高于治疗后1个月;治疗后1个月、3个月、12个月的幼年关节炎活动性系统(JADAS 27)评分均低于治疗前,治疗后3个月、12个月的JADAS 27评分均低于治疗后1个月,治疗后12个月的JADAS 27评分均低于治疗后3个月。41例难治性SoJIA患儿托珠单抗治疗期间无严重不良反应发生。结论:托珠单抗治疗难治性SoJIA可有效改善其临床症状、实验室指标及关节功能,疗效满意且安全性良好。
关键词:托珠单抗 全身型幼年特发性关节炎 疗效 安全性
Efficacy and Safety of Tocilizumab in the Treatment of Refractory Systemic Onset Juvenile Idiopathic Arthritis
Chen Jianfeng Li Qinghua Peng Jianjun
The Third People's Hospital of Jianghan University;
Abstract:Objective: To probe into the efficacy and safety of tocilizumab in the treatment of refractory systemic onset juvenile idiopathic arthritis(SoJIA). Methods: Totally 41 children with refractory SoJIA admitted into our hospital from Jan. 2017 to Jul. 2019 were extracted, and all children were treated with tocilizumab. The clinical manifestations, laboratory indicators and changes of joint function were observed before and after treatment, the efficacy and safety were evaluated. Results: The incidence of fever, rash, lymphadenectasis and arthritis at 1 month, 3 months and 12 months after treatment were lower than those before treatment(P<0.05). Levels of white blood cells(WBC), platelet(PLT), erythrocyte sedimentation rate(ESR) and high-sensitivity C-reactive protein(hsCRP) at 1 month, 3 months and 12 months after treatment were lower than those before treatment(P<0.05), and the level of hemoglobin(Hb) was higher than that before treatment. The levels of WBC and ESR at 3 months and 12 months after treatment were lower than those at 1 month after treatment, while the level of Hb was higher than that at 1 month after treatment. The conversion rates of the American College of Rheumatology(ACR) pediatrics(Ped) function evaluation system ACR Ped 30, 50 and 70 at 3 months and 12 months after treatment were higher than those at 1 month after treatment. The juvenile arthritis disease activity score with 27 joints(JADAS 27) scores at 1 month, 3 months and 12 months after treatment were lower than those before treatment(P<0.05). The JADAS 27 scores at 3 months and 12 months after treatment were lower than those at 1 month after treatment, and the JADAS 27 scores at 12 months after treatment were lower than those at 3 months after treatment. No severe adverse drug reactions occurred during the treatment with tocilizumab in 41 children with refractory SoJIA. Conclusion: The treatment of refractory SoJIA with tolimumab is effective in improving the clinical symptoms, laboratory parameters and joint function with satisfactory efficacy and higher safety.
Keyword:tolimumab; systemic onset juvenile idiopathic arthritis; efficacy; safety;
全身型幼年特发性关节炎(systemic onset juvenile idiopathic arthritis, SoJIA)是儿童时期常见的炎症性疾病之一,临床多表现为发热、皮疹、淋巴结肿大等[1]。相关资料显示[2],幼年特发性关节炎(JIA)中10%~20%为SoJIA,20%~50%的SoJIA患儿可能出现关节畸形、坏死,SoJIA的致死率占JIA的66%左右,是导致JIA患儿致残、致死的最严重的类型,需引起高度重视。SoJIA的常规治疗多为非甾体抗炎药、免疫抑制剂、糖皮质激素等联合治疗,部分难治性SoJIA患儿治疗效果不佳,病情难以控制,且长时间大剂量使用激素会增加不良反应的发生。近年来,随着医学科学的不断发展,发现白细胞介素-6(IL-6)在难治性SoJIA的发病中起到重要作用,托珠单抗是抗IL-6受体的重要人源化单克隆抗体,可有效阻断机体IL-6介导的信号传导,具有较好抗炎效果[3]。虽然已有部分报道托珠单抗在JIA的治疗中取得不错疗效[4-5],但是关于托珠单抗治疗难治性SoJIA的疗效及安全性仍需进一步探究。鉴于此,本研究尝试将托珠单抗应用于难治性SoJIA患儿中,探讨其疗效和优势。
1 资料与方法
1.1 一般资料
选取2017年1月至2019年7月我院收治的41例难治性SoJIA患儿为研究对象,均符合以下纳入及排除标准。其中男23例,女18例,年龄3~11(6.27±1.11)岁,病程为8~40(19.86±3.37)个月。
纳入标准:(1)确诊为难治性SoJIA,伴有关节炎、发热、皮疹等全身性症状,病程≥6个月,非甾体抗炎药、两种或以上免疫抑制剂、激素治疗>3个月效果不佳或激素依赖[6-7];(2)无严重心肺疾病者;(3)肝肾等重要脏器功能正常;(4)首次采用托珠单抗治疗;(5)患儿家属均自愿签署本研究知情同意书。
排除标准:(1)伴有肝炎病毒、潜在结核感染;(2)转至上级医院;(3)伴有血液系统疾病者;(4)伴有细菌、支原体、真菌等活动性感染;(5)伴有免疫缺陷;(6)对治疗药物过敏;(7)依从性差;(8)治疗中途放弃治疗、失访。
1.2 方法
所有难治性SoJIA患儿在原来激素(泼尼松)与免疫抑制剂(甲氨蝶呤、沙利度胺、环孢素、他克莫司)治疗的基础上加用托珠单抗(瑞士罗氏制药,规格80 mg/4 mL),体质量<30 kg患儿剂量为12 mg/kg, 在无菌条件下采用0.9%生理盐水稀释至100 mL,体质量≥30 kg患儿剂量为8 mg/kg, 在无菌条件下采用0.9%生理盐水稀释至 50 mL,均静脉滴注,1次/2周,12周后若疾病维持非活动状态[8]则调整为静脉滴注1次/4周。治疗期间若丙氨酸氨基转移酶升高>正常上限的3倍,则停用托珠单抗。所有患儿均持续治疗12个月,并对患儿进行12个月随访。患儿发热、皮疹、关节炎、淋巴结肿大等临床症状消退,无并发症发生,同时红细胞沉降速率(ESR)、C反应蛋白(CRP)等炎症指标恢复正常,可减停激素和免疫抑制剂。
1.3 观察指标
1.3.1 临床表现
统计所有患儿治疗前、治疗后1个月、治疗后3个月、治疗后12个月发热、皮疹、淋巴结肿大、关节炎情况。
1.3.2 实验室指标
统计所有患儿治疗前、治疗后 1个月、治疗后3个月、治疗后12个月白细胞(WBC)、血红蛋白(Hb)、血小板(PLT)、ESR、超敏C反应蛋白(hsCRP)的变化情况。
1.3.3 关节功能
采用美国风湿病学会(American College of Rheumatology, ACR)儿科(pediatrics, Ped)关节功能评价系统[9]对所有患儿治疗后1个月、3个月、12个月的ACR Ped 30、50、70达标率进行比较。
1.3.4 疗效
采用幼年关节炎活动性系统评分(juvenile arthritis disease activity score with 27 joints, JADAS 27)[10]评价治疗前、治疗后1个月、治疗后3个月、治疗后12个月的疗效。JADAS 27评分系统包括医生对疾病活动度评价、父母-患儿对疾病活动度评价、活动性关节个数及ESR 4个方面,分数越高表示效果越差。
1.3.5 安全性
统计患儿治疗期间出现的不良反应事件,包括转氨酶升高(>参考值上限2倍)[11]、中性粒细胞减少(中性粒细胞计数<1.5×109/L)出血、皮肤异常等发生情况。
1.4 统计学方法
应用SPSS20.0软件,计量资料以x¯±s表示,多组间比较采用方差分析,两组间比较采用t检验,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 治疗前后临床表现
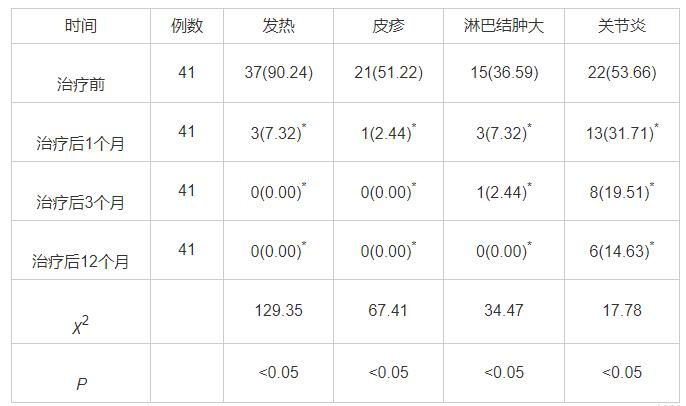
治疗后1个月、3个月、12个月发热、皮疹、淋巴结肿大、关节炎比例均低于治疗前(P<0.05),见表1。
表1 治疗前后临床表现结果 例(%)
2.2 治疗前后实验室指标变化
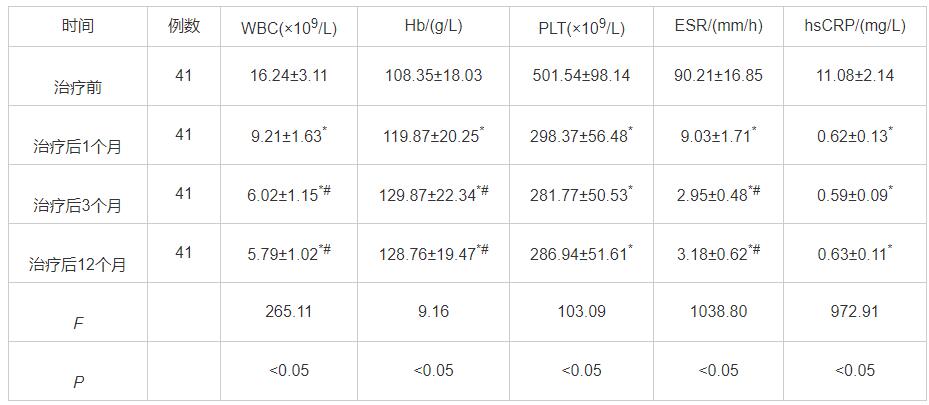
治疗后1个月、3个月、12个月的WBC、PLT、ESR、hsCRP水平均低于治疗前(P<0.05),Hb水平均高于治疗前(P<0.05),其中治疗后3个月、12个月的WBC、ESR水平均低于治疗后1个月(P<0.05),Hb水平均高于治疗后1个月(P<0.05),见表2。
表2 治疗前后实验室指标结果
2.3 患儿治疗前后关节功能变化
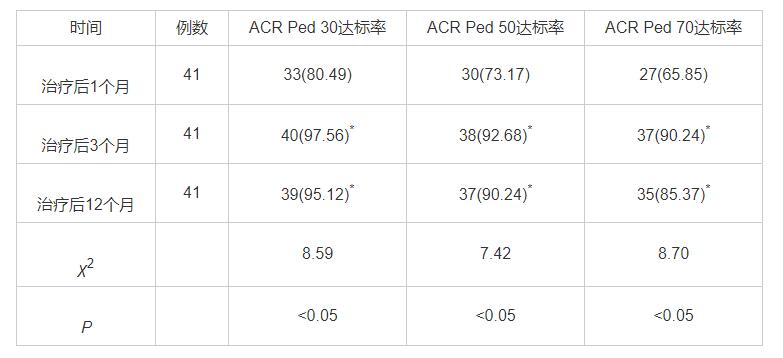
治疗后3个月、12个月ACR Ped 30、50、70达标率均高于治疗后1个月(P<0.05),见表3。
表3 治疗前后关节功能变化结果 例(%)
2.4 治疗前后JADAS 27评分比较
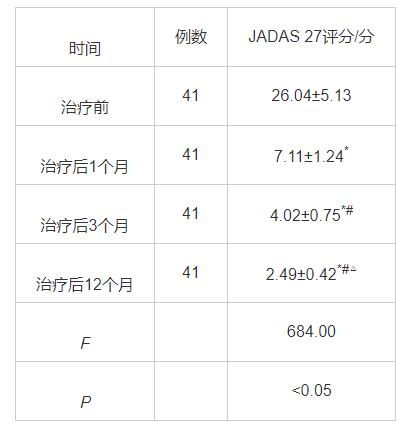
治疗后1个月、3个月、12个月的JADAS 27评分均低于治疗前(P<0.05),治疗后3个月、12个月的JADAS 27评分均低于治疗后1个月(P<0.05),治疗后12个月的JADAS 27评分均低于治疗后3个月(P<0.05),见表4。
表4 治疗前后JADAS 27评分结果
2.5 不良反应发生情况
41例患儿中有3例出现转氨酶升高,2例出现中性粒细胞减少,1例出现皮肤异常,症状轻微,经处理后均好转,无停药情况,无严重不良反应发生。
3 讨论
难治性SoJIA的发病原因主要为自身免疫系统调控紊乱所致,IL-6是机体调控免疫反应中炎性反应的重要细胞因子,IL-6水平与SoJIA患儿病情紧密相关,IL-6可与其受体形成复合物进行信号传导,刺激机体B淋巴细胞产生抗体,刺激T淋巴细胞增殖分化并参与机体全身炎性反应,使用IL-6拮抗剂可有效阻断SoJIA患儿的IL-6信号传导,抑制IL-6活性,有助于改善患儿临床症状[12]。因此,通过控制机体IL-6的表达已成为治疗难治性SoJIA的重要方法。
本研究发现,治疗后1个月、3个月、12个月的发热、皮疹、淋巴结肿大、关节炎的发生率均低于治疗前,说明对难治性SoJIA患儿实施托珠单抗治疗可有效改善其临床症状;治疗后1个月、3个月、12个月的WBC、PLT、ESR、hsCRP水平均低于治疗前,Hb水平均高于治疗前,其中治疗后3个月、12个月的WBC、ESR水平均低于治疗后1个月,Hb水平均高于治疗后1个月,表明对难治性SoJIA患儿实施托珠单抗治疗可有效改善其实验室指标,减轻贫血症状。托珠单抗在SoJIA中的治疗效果已在临床中得到证实,本研究中该药不仅可以有效改善难治性SoJIA患儿的临床症状,促使疾病转化为非活动期,同时还可以明显减少糖皮质激素的剂量,根据难治性SoJIA患儿的病情,所有难治性SoJIA患儿糖皮质激素逐步减少,足量糖皮质激素治疗仅在治疗的第1个月,根据病情活动性评估结果逐渐减少糖皮质激素至最低可接受剂量(每天<0.5 mg/kg),其中有2例患儿持续治疗9个月后去糖皮质激素治疗,3例患儿持续治疗10个月后去糖皮质激素治疗,2例患儿持续治疗12个月后去糖皮质激素治疗。相关研究[13]表明,改善机体缺血状况有利于减轻全身炎症性反应。IL-6可刺激机体生成铁调素,铁调素可通过人体消化系统、巨噬细胞的活性影响机体内铁的含量,托珠单抗可通过阻断难治性SoJIA患儿IL-6受体信号传导,抑制IL-6活性,促进Hb生成,同时IL-6还可刺激巨核细胞的增殖、成熟,从而促进PLT增殖,PLT水平升高是机体发生全身炎性反应的重要表现,托珠单抗发生的免疫阻断可有效抑制难治性SoJIA患儿的炎性反应,促使PLT水平降低[14]。
此外,本研究还发现,治疗后3个月、12个月ACR Ped 30、50、70达标率均高于治疗后1个月,表明对难治性SoJIA患儿实施托珠单抗治疗可有效改善关节功能,效果明显;治疗后1个月、3个月、12个月的JADAS 27评分均低于治疗前,治疗后3个月、12个月的JADAS 27评分均低于治疗后1个月,治疗后12个月的JADAS 27评分均低于治疗后3个月,说明对难治性SoJIA患儿实施托珠单抗治疗可取得满意疗效;41例患儿中有3例出现氨酶升高,2例出现中性粒细胞减少,1例出现皮肤异常,经处理后均好转,表明托珠单抗治疗难治性SoJIA患儿安全性良好,不良反应轻微,对症治疗可缓解,与相关报道[15]结果一致。本研究采用的JADAS 27评分是近期提出的适用于所有类型JIA的复合评价系统,该评价系统具有较好计量特性,并可预测JIA患儿的预后,与ACR Ped具有同等的评价效应,但是与ACR Ped相比JADAS 27评价系统对难治性SoJIA患儿病情及预后具有更加客观的评价[16]。本研究中给予SoJIA患儿托珠单抗治疗,通过结合IL-6受体,阻断IL-6受体信号传导,进而抑制IL-6的生物学活性,达到改善临床症状、减轻炎性反应、改善缺血情况等目的,从而取得满意中长期疗效。相关研究[17]表明,对SoJIA患儿实施托珠单抗治疗效果显著,可有效缓解病情,部分SoJIA患儿停用激素治疗后疾病无复发,与本研究结果共同证实对难治性SoJIA患儿实施托珠单抗治疗可取得满意疗效。
综上所述,托珠单抗治疗难治性SoJIA可有效改善患儿临床症状、实验室指标及关节功能,取得满意疗效且安全性良好。
参考文献
[1] WEI P,HANG S.The value of serum inflammatory factors in early differential diagnosis between systemic-onset juvenile idiopathic arthritis and Kawasaki disease [J].Current immunology,2019,6(5):827-830.
[2] NARENDRA K B.Cyclosporine for systemic onset juvenile idiopathic arthritis:current stand and future directions [J].Indian journal of pediatrics,2019,86(5):576-577.
[3] 苏改秀,黄小兰,周志轩,等.血清细胞因子水平监测在托珠单抗治疗幼年特发性关节炎全身型疗效评价中的应用[J].中华检验医学杂志,2020,43(1):85-90.
[4] 李洪伟,程苏云,唐盈,等.托珠单抗对全身性幼年特发性关节炎一年疗效分析及Janus激酶/信号转导及转录激活因子通路影响[J].中华风湿病学杂志,2019,23(10):666-672.
[5] WANG D D,CHEN X,LI Z P,et al.Treatment of patients with systemic-onset juvenile idiopathic arthritis with tacrolimus [J].Experimental & therapeutic medicine,2019,17(3):2305-2309.
[6] 曾华松.幼年特发性关节炎国际分类标准及治疗[J].实用儿科临床杂志,2011,4(9):721-724.
[7] 吴小川,李灿琳.全身型幼年特发性关节炎发生机制及诊治策略[J].中华实用儿科临床杂志,2017,32(21):1607-1612.
[8] 中国全身型幼年特发性关节炎多中心研究协作组.中国557例全身型幼年特发性关节炎临床特征和预后分析的多中心研究[J].中华风湿病学杂志,2013,17(3):173-178.
[9] RINGOLD S ,ANGELES H,SHEILA T,et al.2019 American college of rheumatology/arthritis foundation guideline for the treatment of juvenile idiopathic arthritis:therapeutic approaches for non-systemic polyarthritis,sacroiliitis,and enthesitis [J].Arthritis care & research,2019,71(6):1-18.
[10] SWART J F,DIJKHUIZEN E H,WULFFRAAT N M,et al.Clinical Juvenile Arthritis Disease Activity Score proves to be a useful tool in treat-to-target therapy in juvenile idiopathic arthritis [J].Annals of the rheumatic diseases,2018,77(3):336-342.
[11] 中华医学会肝病学分会,中华医学会消化病学分会.常用肝脏生物化学试验的临床意义及评价共识[J].中华消化杂志,2010,30(5):331-340.
[12] 陈程,尹薇,刘凡,等.全身型幼年特发性关节炎并可逆性后部白质脑病综合征2例[J].中华实用儿科临床杂志,2019,34(9):708-710.
[13] 李彩凤.重视全身型幼年特发性关节炎的诊治[J].中华实用儿科临床杂志,2018,33(21):1604-1607.
[14] 寻劢,李志辉,段翠蓉,等.托珠单抗治疗12例难治性全身型幼年特发性关节炎的临床疗效[J].儿科药学杂志,2019,25(10):11-15.
[15] TER HAAR N M,TAK T,MOKRY M,et al.Neutrophils in systemic onset Juvenile Idiopathic Arthritis display sepsis-like features which can be reverted by IL-1 blockade [J].Arthritis & rheumatology,2018,70(6):943-956.
[16] SURI D,VIGNESH P,ANJANI G,et al.LACC1 gene mutation in three sisters with polyarthritis without systemic features [J].Annals of the rheumatic diseases,2019,79(3):216-220.
[17] 耿玲玲,苗峰,周扬,等.托珠单抗治疗难治性全身型幼年特发性关节炎16例中长期疗效及安全性观察[J].中国实用儿科杂志,2019,34(1):37-40.
热门排行


